【文獻解讀】辛伐他汀可阻止大鼠中由肝硬化門脈高壓導致的慢加急性肝衰竭
日期:2018-08-09 16:07:36
Part I明星產品
產品名稱:大鼠中性粒細胞明膠酶相關脂質運載蛋白(NGAL)ELISA Kit
產品貨號:CSB-E09409r
種屬: Rattus norvegicus (Rat)
檢測范圍: 0.312 ng/mL-20 ng/mL
靈敏度: 0.078 ng/mL

Part II 文獻詳情
題目:Simvastatin Prevents Progression of Acute on Chronic Liver Failure in Rats With Cirrhosis and Portal Hypertension辛伐他汀可阻止大鼠中由肝硬化門脈高壓導致的慢加急性肝衰竭
期刊:Gastroenterology
影響因子:20.773
研究背景及目的:
細菌感染可加快肝硬化及其臨床病變,最終發展成慢加急性肝衰竭(ACLF)。ACLF主要臨床表現包括急性失代償,器官衰竭和短時期內的高死亡率。由于對肝硬化患者ACLF細胞和分子機制知之甚少,因此一直沒有有效的治療手段。在本研究中,Dinesh Mani Tripathi和他的小伙伴們開發了一種與敗血癥相關的ACLF臨床前模型,以便于ACLF發病機制的研究及辛伐他汀抗ACLF作用的評估。
結論:
1、在對肝硬化大鼠的研究中,作者發現LPS可以促進ACLF的發生發展,加重慢性肝病的并發癥并減少存活時間。
2、辛伐他汀可減輕LPS誘導的ACLF大鼠的炎癥和肝損傷,支持其用于治療晚期慢性肝病患者。
結果:
- LPS可通過加劇肝內微血管功能障礙、肝臟炎癥與氧化應激,同時增加肝星狀細胞和中性粒細胞,進一步加重肝硬化大鼠的門靜脈高壓癥。
- 肝硬化大鼠經LPS處理后,其存活時間明顯短于肝硬化大鼠對照組。
- 辛伐他汀可預防大多數ACLF并發癥并增加存活時間。此外,實驗結果還表明,辛伐他汀可增強肝竇功能,降低門脈高壓和炎癥及氧化指標。
- 該藥物顯著降低轉氨酶,總膽紅素和氨的水平,有效抑制LPS介導的肝硬化大鼠肝組織中HSC的活化。
1、外源性給予LPS對肝硬化大鼠的全身作用
本研究中,向肝硬化動物給予外源性LPS可以顯著升高內毒素血癥,而內毒素血癥與全身血液動力學和腎功能障礙息息相關(Suppl. Fig 2)。
2、LPS可加重肝硬化大鼠的門靜脈高壓癥和肝臟微循環功能障礙,而辛伐他汀可預防ACLF的不良反應
與空白組相比,失代償和代償性CCl4肝硬化大鼠腹腔注射LPS后,其門靜脈壓力(PP)呈顯著增加趨勢,在代償性TAA肝硬化動物中也觀察到相似結果(表1a),但門靜脈血流(PBF)有顯著變化,因此作者推斷ACLF門靜脈高壓增加是由于肝血管阻力(HVR)增高所致。同樣,作者在靜脈注射LPS的處理組中也觀察到了類似的結果(Supple. Table 3)。另外,在離體肝臟微循環分析中,作者觀察到LPS處理組的門靜脈灌注壓顯著增加(Fig 1 top),并且肝血管擴張對乙酰膽堿的反應減弱(Fig 1 bottom),這也進一步證實了肝臟微血管功能障礙會隨著ACLF患病時間推移而加重。
ACLF相關潛在干預治療研究表明,辛伐他汀可以有效的阻止LPS誘導的門靜脈高壓惡化。如Table 1a所示,與LPS處理組相比,辛伐他汀治療組的PP明顯降低,此時也并未觀察到PBF的變化,這也進一步表明HVR降低是PP改善的原因。事實上,在失代償性CCl4大鼠中,HVR對辛伐他汀的敏感度降低,但這一現象并未在BDL動物中觀察到。盡管在CCl4代償性肝硬化動物中,辛伐他汀處理組的PBF或HVR沒有顯著變化,但有趣的是MAP卻略有改善。這與體內觀察到的改善相一致。此外,辛伐他汀還可以防止LPS誘導的ACLF在離體門靜脈灌注壓(Fig 1 top)和肝血管擴張反應中對乙酰膽堿的血流動力學惡化(Fig 1 bottom)。
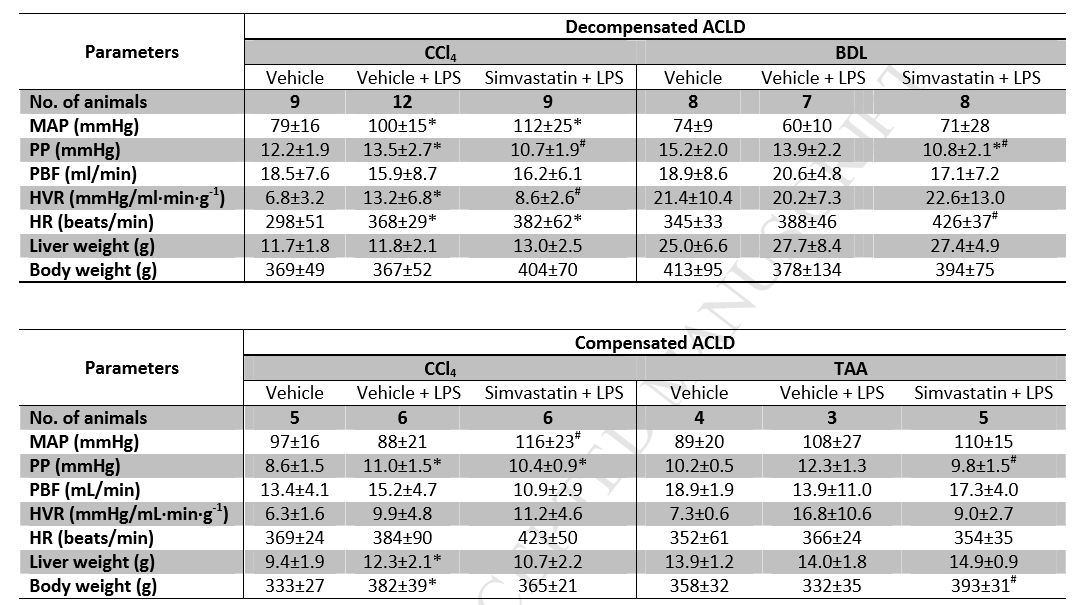
Table 1a LPS和辛伐他汀對失代償性和代償性晚期慢性肝病(ACLD)大鼠肝臟和全身血流動力學的影響
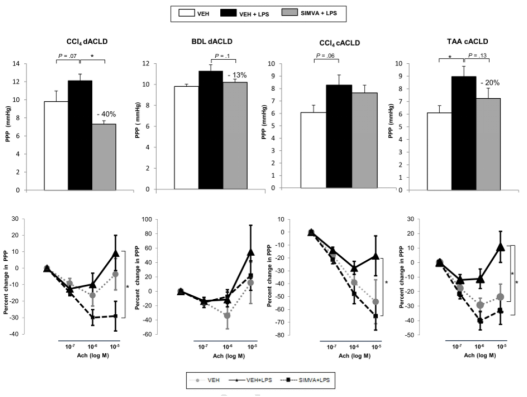
圖1:辛伐他汀對晚期慢性肝病(ACLD)大鼠的肝微血管功能的影響
3、他汀類藥物可以有效緩解ACLF所引起的驗證及氧化應激進一步加劇
如Fig 2,Suppl. Fig 3和Suppl. Fig 4所示,作者通過檢測促炎與抗炎因子的變化發現LPS可以顯著促進肝硬化大鼠全身和肝臟炎癥進一步惡化。同時作者通過觀察NETs的形成,發現這種炎性爆發與肝臟中性粒細胞浸潤和中性粒細胞活性的顯著增加有關(Fig 3和Suppl. Fig 5)。如Fig 2和Fig 3所示,辛伐他汀可預防失代償性肝硬化大鼠因內毒素血癥引起的炎癥性爆發,盡管其抗炎作用在BDL臨床前模型中不太明顯(Fig2-3和supple. Fig 3-4)。在補償的CCl4大鼠中也觀察到類似的趨勢(Suppl. Fig 5)。
如Fig 4A-B所示,LPS處理組過氧化物水平顯著升高及過氧亞硝酸鹽的非顯著增加,說明LPS加劇了失代償性肝硬化大鼠的肝臟氧化應激。有趣的是,氧化解除與肝eNOS活性明顯降低有關(Fig 4C-D)。辛伐他汀在失代償性肝硬化模型(Fig 4A-4B)和CCl4模型(fFig 4C)中均能抑制ACLF所致氧化應激的增加(Fig 4A-4B),并改善P-eNOS/eNOS的比值(Fig 4C),但對BDL模型(Fig 4D)則無明顯影響。
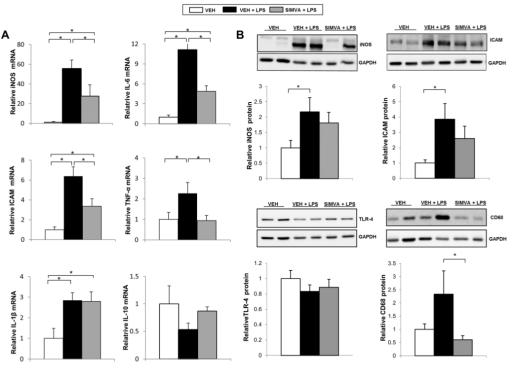
Fig 2. ACLF失代償性ACLD大鼠的肝臟炎癥
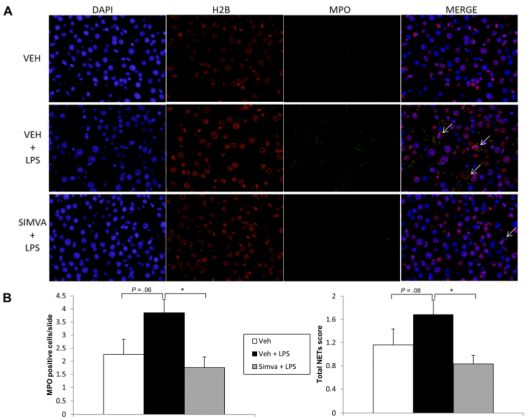
Fig 3. 失代償期ACLF失代償性ACLD大鼠中性粒細胞和NETs的檢測
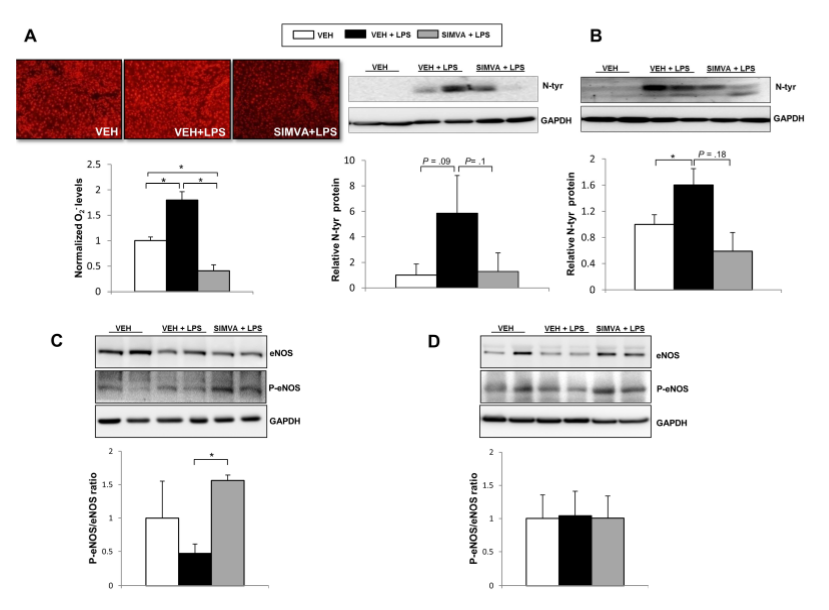
Fig 4. 辛伐他汀對ACLF失代償性肝硬化大鼠氧化應激和NO通路的影響
4、辛伐他汀可以改善由LPS導致的肝狀星性細胞表型惡化現象
通過對ACLF期間肝微循環惡化分子機制的進一步研究,作者發現肝臟中α-SMA蛋白表達和mRNA水平均顯著上調,表明內毒素血癥可以使失代償性肝硬化動物HSC急性活化(Fig. 5)。盡管辛伐他汀沒有改變肝纖維化(數據未顯示),但在兩種失代償的肝硬化大鼠模型中LPS介導的HSC活化都得到了有效的改善。此外,考慮到ACLF期間中性粒細胞浸潤增加,作者對LPS激活的中性粒細胞是否影響HSC表型進行了驗證。如Suppl. Fig 6 所示,活化的嗜中性粒細胞與LX2細胞的直接共培養會引起HSC過度活化,但在間接共培養卻并未觀察到HSC過度活化。有趣的是,LPS刺激的中性粒細胞對LX2表型的不利影響卻在辛伐他汀的作用下得到了有效改善(Supple. Fig 6),表明在LPS誘導ACLF過程中,中性粒細胞可能部分介導HSC的激活。
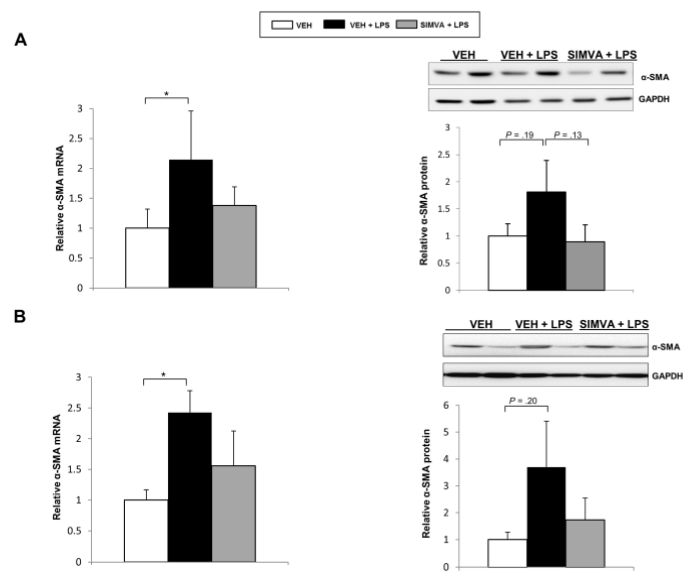
Fig. 5 辛伐他汀對晚期慢性肝病(ACLD)大鼠肝星狀細胞表型的影響
5、辛伐他汀可以改善ACLF對肝硬化動物存活率的消極影響
首先,作者對LPS處理后4或24小時(分別在失代償和代償性的肝硬化動物中)大鼠存活進行了監測。統計結果顯示,非ACLF失代償和代償性肝硬化動物無死亡。相反,LPS治療組,尤其是失代償性肝硬化模型組死亡率明顯高于對照組(Fig 2),如Table 1b所示,通過對存活大鼠中生化指標的監測, LPS可以顯著惡化ACLF的作用得到了進一步證實。重要的是,辛伐他汀預處理能有效改善失代償性肝硬化模型中LPS誘導的ACLF的存活率(Table 2),并顯著降低轉氨酶、總膽紅素和氨含量(Table 1b)。代償性肝硬化大鼠(Table 1b和Table 2)也有類似的趨勢。

Table 1b LPS和辛伐他汀對失代償和補償性ACLD大鼠生化指標的影響
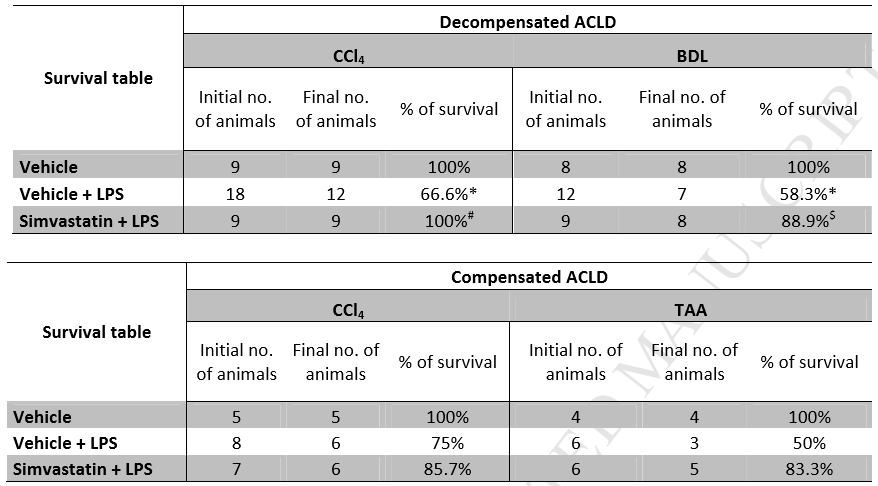
Table 2失代償和補償性ACLD大鼠的初始和最終動物數量和存活率
討論:
由于LPS施用導致的ACLF的發展同時顯著加劇肝臟和全身炎癥,導致已經功能失調的肝微血管系統的嚴重惡化和肝硬化動物的存活率明顯降低。辛伐他汀主要通過避免炎癥性爆發,氧化應激和竇狀細胞功能障礙來預防這些失調。綜合本次和之前的研究結果,作者建議辛伐他汀作為接受ACLF的肝硬化患者的安全且有用的治療策略。 實際上,大規模臨床試驗將評估該化合物對失代償期肝硬化患者的可能有益作用。












